من انهيار الأحماض الدهنية يعمل على توليد الطاقة في الخلايا ويتم عبر ما يعرف بأكسدة بيتا. في سياق أكسدة بيتا ، يتشكل أسيتيل أنزيم أ ، والذي يتفكك إلى ثاني أكسيد الكربون والماء أو يعيد تغذية دورة حمض الستريك. يمكن أن تؤدي الاضطرابات في تكسير الأحماض الدهنية إلى أمراض خطيرة.
ما هو تكسير الأحماض الدهنية؟

إلى جانب تكسير الجلوكوز في الكائن الحي ، فإن تكسير الأحماض الدهنية هو عملية التمثيل الغذائي الهامة لتوليد الطاقة في الخلية.
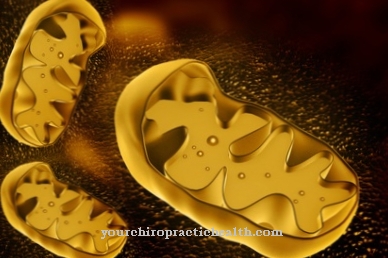
يتم تكسير الأحماض الدهنية في الميتوكوندريا. يحدث التحلل عن طريق ما يسمى بأكسدة بيتا. نشأ مصطلح "بيتا" من حقيقة أن الأكسدة تحدث على ذرة الكربون الثالثة (ذرة كربون بيتا) لجزيء الأحماض الدهنية.
في نهاية دورة الأكسدة ، تنقسم ذرتان من الكربون على شكل حمض أسيتيك منشط (أسيتيل أنزيم أ). نظرًا لأن تكسير الأحماض الدهنية يتطلب عدة دورات أكسدة ، فقد كانت العملية تُعرف سابقًا أيضًا باسم دوامة الأحماض الدهنية.
يتم تكسير أنزيم الأسيتيل بشكل أكبر في الميتوكوندريا إلى أجسام الكيتون أو ثاني أكسيد الكربون والماء. عندما يعود إلى السيتوبلازم من الميتوكوندريا ، يتم إعادته إلى دورة حمض الستريك.
يتم إنتاج المزيد من الطاقة في تكسير الأحماض الدهنية مقارنة بحرق الجلوكوز.
الوظيفة والمهمة
يحدث تكسير الأحماض الدهنية في عدة خطوات تفاعل ويحدث داخل الميتوكوندريا.بادئ ذي بدء ، توجد جزيئات الأحماض الدهنية في العصارة الخلوية للخلية.
إنها جزيئات خاملة يجب أولاً تنشيطها للتحلل ونقلها إلى الميتوكوندريا. لتنشيط الأحماض الدهنية ، يتم نقل الإنزيم المساعد A بتكوين أسيل CoA. أولاً ، يتم تقسيم ATP إلى بيروفوسفات و AMP. ثم يتم استخدام AMP لتكوين acyl AMP (acyl adenylate).
بعد فصل AMP ، يمكن أسترة الحمض الدهني باستخدام الإنزيم المساعد A لتكوين أسيل- CoA. بعد ذلك ، بمساعدة إنزيم كارنيتين أسيل ترانسفيراز I ، يتم نقل الكارنيتين إلى الأحماض الدهنية المنشط.
يتم نقل هذا المركب إلى الميتوكوندريا (مصفوفة الميتوكوندريا) بواسطة ناقل كارنيتين-أسيل كارنيتين (CACT). هناك ، ينقسم الكارنيتين مرة أخرى وينتقل الإنزيم المساعد أ مرة أخرى ، ويتم إخراج الكارنيتين من المصفوفة ويتوفر أسيل- CoA في الميتوكوندريا من أجل أكسدة بيتا الفعلية.
تحدث أكسدة بيتا الفعلية في أربع خطوات تفاعل. تتم خطوات الأكسدة التقليدية مع الأحماض الدهنية المشبعة ذات الأرقام الزوجية. إذا تم تكسير الأحماض الدهنية ذات الأرقام الفردية أو غير المشبعة ، فيجب أولاً تحضير جزيء البداية لأكسدة بيتا من خلال تفاعلات أخرى.
يتأكسد أسيل- CoA للأحماض الدهنية المشبعة ذات الأرقام الزوجية في خطوة التفاعل الأولى بمساعدة إنزيم أسيل- CoA dehydrogenase. هذا يخلق رابطة مزدوجة بين ذرة الكربون الثانية والثالثة في موضع الترانس. بالإضافة إلى ذلك ، يتم تحويل FAD إلى FADH2.
عادة ، تكون الروابط المزدوجة للأحماض الدهنية غير المشبعة في وضع رابطة الدول المستقلة ، لكن الخطوة التالية في تفاعل تحلل الأحماض الدهنية لا يمكن أن تحدث إلا برابطة مزدوجة في موضع الترانس.
في خطوة التفاعل الثانية ، يضيف إنزيم enoyl-CoA hydratase جزيء ماء إلى ذرة كربون بيتا لتشكيل مجموعة هيدروكسيل. يقوم ما يسمى بـ L-3-hydroxyacyl-CoA dehydrogenase بعد ذلك بأكسدة ذرة كربون بيتا إلى مجموعة كيتو. يتكون 3-Ketoacyl-CoA.
في خطوة التفاعل الأخيرة ، يرتبط الإنزيم الإضافي A بذرة كربون بيتا. ينقسم Acetyl-CoA (حمض الأسيتيك المنشط) ويتبقى أسيل- CoA وهو عبارة عن ذرتين من الكربون أقصر. يمر هذا الجزيء المتبقي الأقصر خلال دورة التفاعل التالية وصولاً إلى انقسام آخر من أسيتيل CoA.
تستمر العملية حتى يتم تقسيم الجزيء بأكمله إلى حمض الأسيتيك المنشط. قد تكون العملية العكسية لأكسدة بيتا ممكنة أيضًا من الناحية النظرية ، لكنها لا تحدث في الطبيعة.
هناك آلية تفاعل مختلفة لتخليق الأحماض الدهنية. في الميتوكوندريا ، يتم تكسير الأسيتيل CoA إلى ثاني أكسيد الكربون والماء أو في أجسام الكيتون مع إطلاق الطاقة. في حالة الأحماض الدهنية ذات الأرقام الفردية ، يظل propionyl-CoA بثلاث ذرات كربون في النهاية. هذا الجزيء ينقسم بطريقة مختلفة.
عندما يتم تكسير الأحماض الدهنية غير المشبعة ، يتم تحويل الروابط المزدوجة من تكوينات رابطة الدول المستقلة إلى تكوينات غير مشبعة بواسطة متماكبات محددة.
الامراض والاعتلالات
اضطرابات تكسير الأحماض الدهنية نادرة الحدوث ، ولكنها قد تؤدي إلى مشاكل صحية خطيرة. دائمًا تقريبًا ، هذه أمراض وراثية.
هناك طفرة جينية مقابلة لكل إنزيم ذي صلة تقريبًا يشارك في تكسير الأحماض الدهنية. على سبيل المثال ، ينشأ النقص في إنزيم MCAD من طفرة جينية موروثة بطريقة جسمية متنحية. MCAD مسؤول عن تكسير الأحماض الدهنية متوسطة السلسلة. تشمل الأعراض نقص السكر في الدم (انخفاض السكر في الدم) ، والنوبات ، وحالات الغيبوبة المتكررة. نظرًا لأنه لا يمكن استخدام الأحماض الدهنية لتوليد الطاقة هنا ، يتم حرق مستويات متزايدة من الجلوكوز. وهذا يؤدي إلى نقص سكر الدم وخطر الإصابة بالغيبوبة.
نظرًا لأنه يجب دائمًا تزويد الجسم بالجلوكوز لإنتاج الطاقة ، يجب ألا يكون هناك امتناع طويل الأمد عن الطعام. إذا لزم الأمر ، يجب إعطاء جرعة عالية من الجلوكوز في حالة أزمة حادة.
علاوة على ذلك ، تعتبر جميع الاعتلالات العضلية من سمات اضطرابات تحلل الأحماض الدهنية في الميتوكوندريا. هذا يؤدي إلى ضعف العضلات واضطرابات التمثيل الغذائي للكبد وظروف سكر الدم. ما يصل إلى 70 في المائة من المصابين يصابون بالعمى في مجرى حياتهم.
تحدث الأمراض الخطيرة أيضًا عند حدوث اضطراب في تحلل الأحماض الدهنية الطويلة جدًا. لا يتم تكسير هذه الأحماض الدهنية طويلة السلسلة في الميتوكوندريا ولكن في البيروكسيسومات. هنا يكون الإنزيم ALDP مسؤولاً عن إدخال البيروكسيسومات. ومع ذلك ، عندما يكون ALDP معيبًا ، تتراكم جزيئات الأحماض الدهنية الطويلة في السيتوبلازم وبالتالي تؤدي إلى اضطرابات استقلابية شديدة. كما تتعرض الخلايا العصبية والمادة البيضاء في الدماغ للهجوم. هذا النوع من اضطراب انهيار الأحماض الدهنية يؤدي إلى أعراض عصبية مثل اضطرابات التوازن ، والتنميل ، والتشنجات ، والغدد الكظرية غير النشطة.