كيموكينيس هي بروتينات إشارة صغيرة تحفز الانجذاب الكيميائي (الهجرة) للخلايا. عادة هذه الخلايا هي خلايا مناعية. وبالتالي ، فإن الكيموكينات مسؤولة عن الأداء الفعال لجهاز المناعة.
ما هي الكيموكينات؟
الكيموكينات هي بروتينات صغيرة تنتمي إلى عائلة السيتوكينات. تسبب هجرة الخلايا. بشكل أساسي ، هذه هي الخلايا المناعية التي من المفترض أن تصل بسرعة إلى الموقع المناسب للإصابة أو العدوى.
يتم إنتاج الكيموكينات بواسطة الخلايا التي من المفترض أن تجذبها. توجد على سطح هذه الخلايا مستقبلات تمكن الكيميائيات من الالتحام. تنقسم جزيئات الإشارة إلى كيموكينات التهابية وتماثلية. في معظم الحالات ، تكون الكيموكينات التهابية. إنها تجذب الخلايا المناعية إلى وجهتها ، مما يؤدي على الفور إلى حدوث عمليات التهابية للدفاع عن نفسها ضد العدوى. دائمًا ما يتم إنتاج الكيموكينات الالتهابية في موقع الإصابة أو العدوى بواسطة الخلايا المناعية الموجودة هناك لجذب المزيد من الخلايا الدفاعية.
يتم إنتاج الكيماويات المتجانسة باستمرار حتى في حالة عدم وجود عدوى. يتم استخدامها لمراقبة الأنسجة السليمة. للكيماويات تأثير كيميائي كيميائي على الخلايا المناعية مثل الخلايا الوحيدة ، الضامة ، الخلايا الكيراتينية ، الخلايا الليفية ، الصفائح الدموية ، الخلايا البطانية ، الخلايا التائية ، الخلايا الفغرة ، العدلات ، والخلايا المتغصنة. يتم إنتاجها أيضًا بواسطة هذه الخلايا كمواد إشارات لجذب خلايا مماثلة إذا لزم الأمر.
التشريح والهيكل
الكيموكينات هي سلاسل بروتينية صغيرة تحتوي كل منها على 75 إلى 125 من الأحماض الأمينية. يوجد في الطرف النهائي للسلسلة واحد أو اثنين من بقايا السيستين. السيستين هو حمض أميني يحتوي على الكبريت ويمكن أن يشكل جسور ثاني كبريتيد في الجزيء. تشكل بقايا السيستين الآن جسور الكبريتيد داخل سلسلة البروتين.
في حين أن تسلسل الأحماض الأمينية متغير داخل بروتينات عائلة الكيموكين ، فإن البنية الثلاثية تظل كما هي بالنسبة لجميع الكيموكينات. يتكون الجسم الرئيسي على شكل صفيحة ثلاثية الأضلاع متوازية مع هيكل بيتا. تنتهي السلسلة عند نهاية الكربوكسي مع حلزون ألفا. توجد الآن بقايا السيستين. هناك أربعة هياكل يمكن فيها ترتيب بقايا السيستين الطرفية. كل هيكل يرمز إلى عائلة من الكيميائيات. لذلك يمكن أن يتبع اثنان من بقايا السيستين بعضهما البعض. تسمى عائلة chemokine المقابلة عائلة CC. إذا تم تبديل حمض أميني آخر بين بقايا السيستين ، فهو عائلة CXC. تحتوي عائلة CX3C على بقايا سيستين مفصولة بثلاثة أحماض أمينية.
أخيرًا ، هناك عائلة بها بقايا السيستين المعروفة باسم عائلة C. تشكل جميع بقايا السيستين جسرًا كبريتيدًا داخل السلسلة. العائلات الكيميائية الفردية لها وظائف مختلفة. لا يزال الهيكل الدقيق للكيماويات غير مفهومة تمامًا. لا تحتاج الكيموكينات بالضرورة إلى سوائل الأنسجة أو الدم لأداء وظيفتها. يمكنهم أيضًا تمرير إشاراتهم عبر الهياكل الصلبة من خلال تدرجات التركيز. مع الشحنة الموجبة للعديد من الأحماض الأمينية الأساسية ، فإنها ترتبط بجزيء سكر سالب الشحنة (جليكوزامينوجلوكان) على سطح الخلايا. لم يتضح بعد سبب فقدانهم لوظائفهم عندما لم يعد بإمكانهم الارتباط بالجليكوزامينوجلوكان.
الوظيفة والمهام
تتمثل الوظيفة الرئيسية للكيموكينات في جذب خلايا مناعية معينة إلى أماكن في الجسم تخضع حاليًا لمستوى أعلى من الدفاع ضد المتطفلين المعديين. هذا يجعل الاستجابة المناعية أكثر فعالية. في معظم الحالات ، يتأكدون أيضًا من حدوث تفاعلات التهابية كبيرة لدرء العدوى. يتم إنشاؤها في موقع الإصابة أو العدوى بواسطة الخلايا المناعية الموجودة بالفعل هناك.
تتحرك الخلايا المنجذبة الآن نحو أعلى تركيز للكيموكينات. توجد المستقبلات الكيميائية المقابلة على سطحها. ترتبط الكيموكينات بهذه المستقبلات وبالتالي تحفز هجرة الخلايا نحو أعلى تركيز كيميائي. ومع ذلك ، فإن كل عائلة كيموكين ترتبط بمستقبلاتها الخاصة.تضمن عائلة CC هجرة الخلايا الأحادية والخلايا الليمفاوية وكذلك الخلايا القاعدية والحمضات. عائلة CXC مسؤولة عن تولد الأوعية (نمو الأوعية الدموية). تلعب عائلة CX3C دورًا في العمليات الالتهابية في الجهاز العصبي. أخيرًا ، تعمل الكيميائيات C على تنشيط خلايا CD8 T وخلايا NK (الخلايا القاتلة الطبيعية).
يمكنك العثور على أدويتك هنا
➔ أدوية لتقوية جهاز المناعةالأمراض
إذا تعطل تفاعل الكيموكينات ومستقبلات الكيموكين ، فإن الجهاز المناعي يتعطل. في كثير من الأحيان ، بسبب طفرة في المستقبل المقابل ، لم تعد مناسبة تمامًا لرسو الكيميائيات. هذا يعني أنه لم يعد من الممكن جذب الخلايا المناعية في المواقف الحرجة.
ثم يتجلى هذا الخلل في شكل نقص المناعة. يمكن إرجاع ما يسمى بمتلازمة WHIM ، وهو نقص مناعي خاص ، إلى عيب في مستقبلات الكيموكين. يتجلى هذا المرض في تكرار الالتهابات الفيروسية والبكتيرية. يُظهر المرضى قابلية خاصة للإصابة بفيروس الورم الحليمي البشري ، حيث يتم التعبير عن العدوى بالثآليل. نخاع العظم مليء بالخلايا السليفة التائية ، لكنها لا تهاجر إلى مواقع الإصابة. من الممكن أيضًا حدوث نقص في المناعة الانتقائية ضد بعض مسببات الأمراض. على سبيل المثال ، إذا تم تحور أحد المستقبلات الكيميائية لعائلة CC ، فهناك قابلية خاصة للإصابة بفيروس غرب النيل. في حالة حدوث طفرة ، يضمن نفس المستقبل أيضًا مناعة وراثية لفيروس HI.
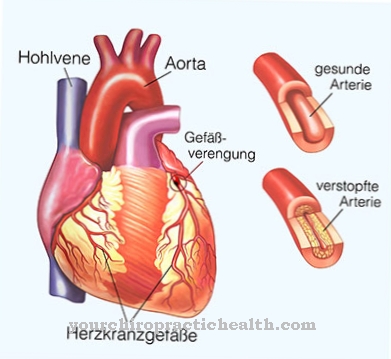
يمكن أن تكون بعض الطفرات في منطقة المستقبلات الكيميائية مسؤولة جزئيًا عن أمراض المناعة الذاتية أو الحساسية. يمكن أن يؤدي الإفراط في إنتاج بعض الكيميائيات أيضًا إلى المرض. وجد أن تطور الصدفية (الصدفية) مرتبط بالإفراط في إنتاج CXC chemokine IL-8. يحدث التهاب المفاصل الروماتويدي أيضًا جنبًا إلى جنب مع الإفراط في إنتاج IL-8. غالبًا ما تكون تغيرات تصلب الشرايين نتيجة لعمليات الالتهاب المفرط ، والتي تحدث أحيانًا بسبب زيادة أنشطة الكيماويات.






.jpg)